- 化学平衡建立的过程
- 共29题
一定条件下,通过下列反应可以制备特种陶瓷的原料
正确答案
解析
该反应为正方向体积增加且吸热。A、升高温度,平衡正向移动,气体的质量增加,密度增大,正确;B、增加co的量,平衡正向移动,但压强增大,转化的量,没有上一平衡多,故比值减小,错误;C、平衡常数只与温度有关,错误;D因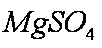
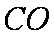
知识点
合成氨尿素工业生产过程中涉及到的物质转化过程如下图所示。
(1)天然气在高温、催化剂作用下与水蒸气反应生成H2和CO的化学方程式为 。
(2)在合成氨生产中,将生成的氨及时从反应后的气体中分离出来。运用化学平衡的
知识分析这样做的是否有利于氨的合成
(3)右图为合成氨反应在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积比为1:3时,平衡混合物中氨的体积分数。
①若分别用υA(NH3)和υB(NH3)表示从反应开始至达平衡状态A、B时的化学反应速率,则υA(NH3) υB(NH3)(填“>”、“<”或“=”)。
②在相同温度、当压强由p1变为p3时,合成氨
反应的化学平衡常数 。(填“变大”、“变小”或“不变”)。
③在250℃、1.0×104 kPa下,H2的转化率为 %(计算结果保留小数点后
1位)。
(4)NH3(g) 与CO2(g) 经过两步反应生成尿素,
NH3(g) 与CO2(g) 反应生成尿素的热化学方程式为 。
(5)运输氨时,不能使用铜及其合金制造的管道阀门。因为,在潮湿的环境中,金属
铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,该反应的离子方程
式为 。
正确答案
见解析。
解析
(1)
(2)移走氨气,减小生成物浓度,平衡右移,有利于氨生成
(3)① <
② 不变
③ 66.7%
(4)2NH3(g) + CO2(g) === CO(NH2)2(s) + H2O(l) △H = -134 kJ/mol
(5)2Cu + 8NH3 + O2 + 2H2O === 2Cu(NH3)42+ + 4OH-
知识点
邻羟基桂皮酸是合成香精的重要原料,下为合成邻羟基桂皮酸的路线之一:
试回答下列问题:
(1)化合物Ⅰ的名称是 ;化合物II→化合物III 的有机反应类型: ;
(2)化合物III 在银氨溶液中发生反应化学方程式: ;
(3)有机物 X 为化合物IV的同分异构体,且知有机物X 有如下特点:
①苯环上的氢有两种,②能与NaHCO3 反应放出气体,③能发生银镜反应。
请写出两种化合物X的结构简式_____________________、___________________________
(4)下列说法正确的是 ;
a.化合物I遇氯化铁溶液呈紫色
b.化合物II能与NaHCO3溶液反应
c.1mol化合物IV完全燃烧消耗 9.5molO2
d.1mol化合物III最多能与3 molH2 反应
(5)有机物R(C9H9ClO3)经过反应也可制得化合物IV,则 R 在NaOH 醇溶液中反应的化学方程式为 。
正确答案
(1)邻羟基苯甲醛;消去反应(2 分)
(2)
(3 分)
(3)
(每个2分,共4分)
(4)a 、c (4 分)
(5)
(3 分)
或
解析
略
知识点
对于可逆反应H2(g)+I2(g)≒2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是
正确答案
解析
A选项中,速率之比等于计量数之比,应为1:2;B选项出现的净速率在中学没出现过,但根据平均速率的求算,为反应物的净减少量,该项正确;C项明显错误,反应过程中,正反应速率是减小的过程,而逆反应速率是增大的过程;D选项是平衡定义中来,正确。
知识点
往含0.2mol NaOH和0.1mol Ca(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为6.72L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计)
正确答案
解析
略
知识点
扫码查看完整答案与解析











